
Fig. 1 抗体药开发的一般流程



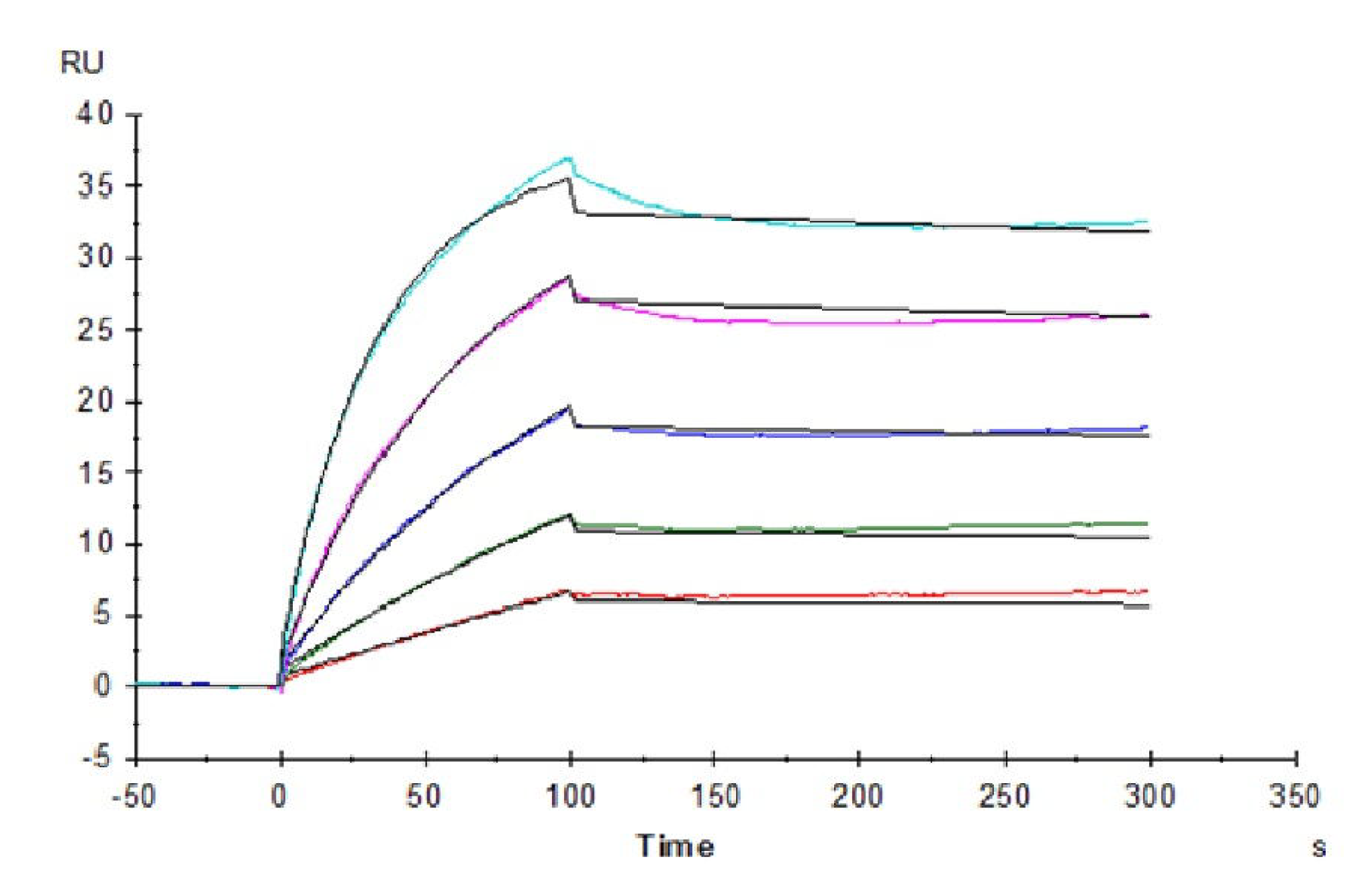


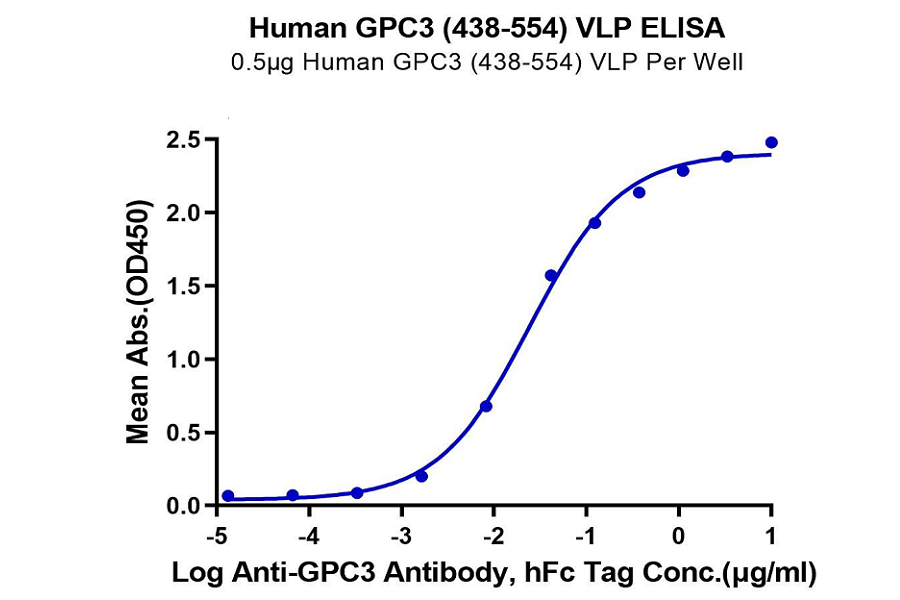




获得抗体后,需对所得抗体进行筛选与优化。生物素标记的蛋白因具有更高的灵敏度和特异性,不仅可用于各种检测分析,也可用于免疫捕获,在ELISA、SPR、流式及生物淘选等分析中具有特殊优势。
恺佧生物提供定点和非定点生物素化蛋白以供客户进行抗体筛选检测。其中,定点生物素化蛋白利用Avi标签上赖氨酸残基可被生物素连接酶BirA修饰上生物素的原理,能实现精准的生物素修饰操控,且蛋白固定到亲和素包被的表面时具有方向一致性,被广泛应用于各类检测分析中。


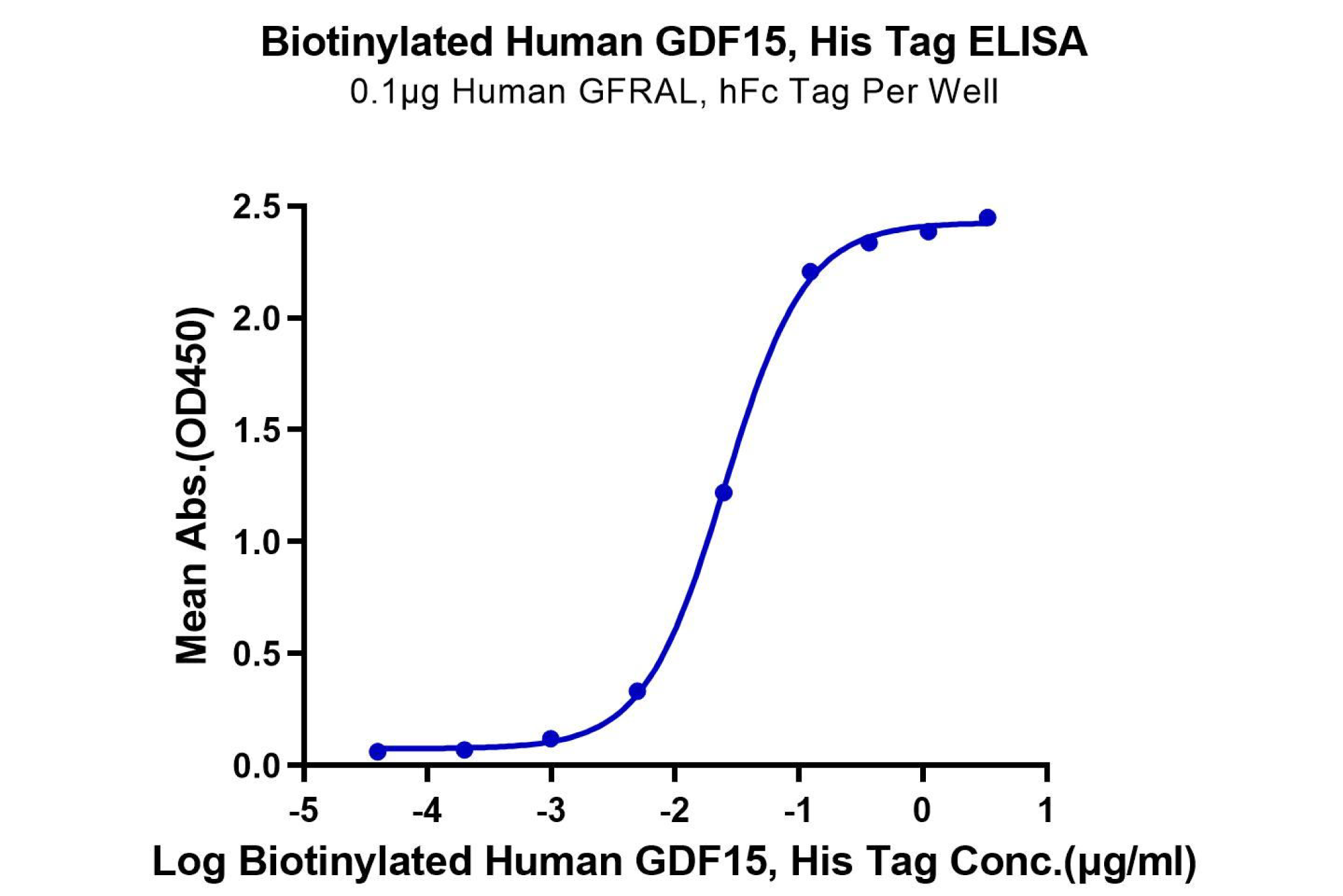
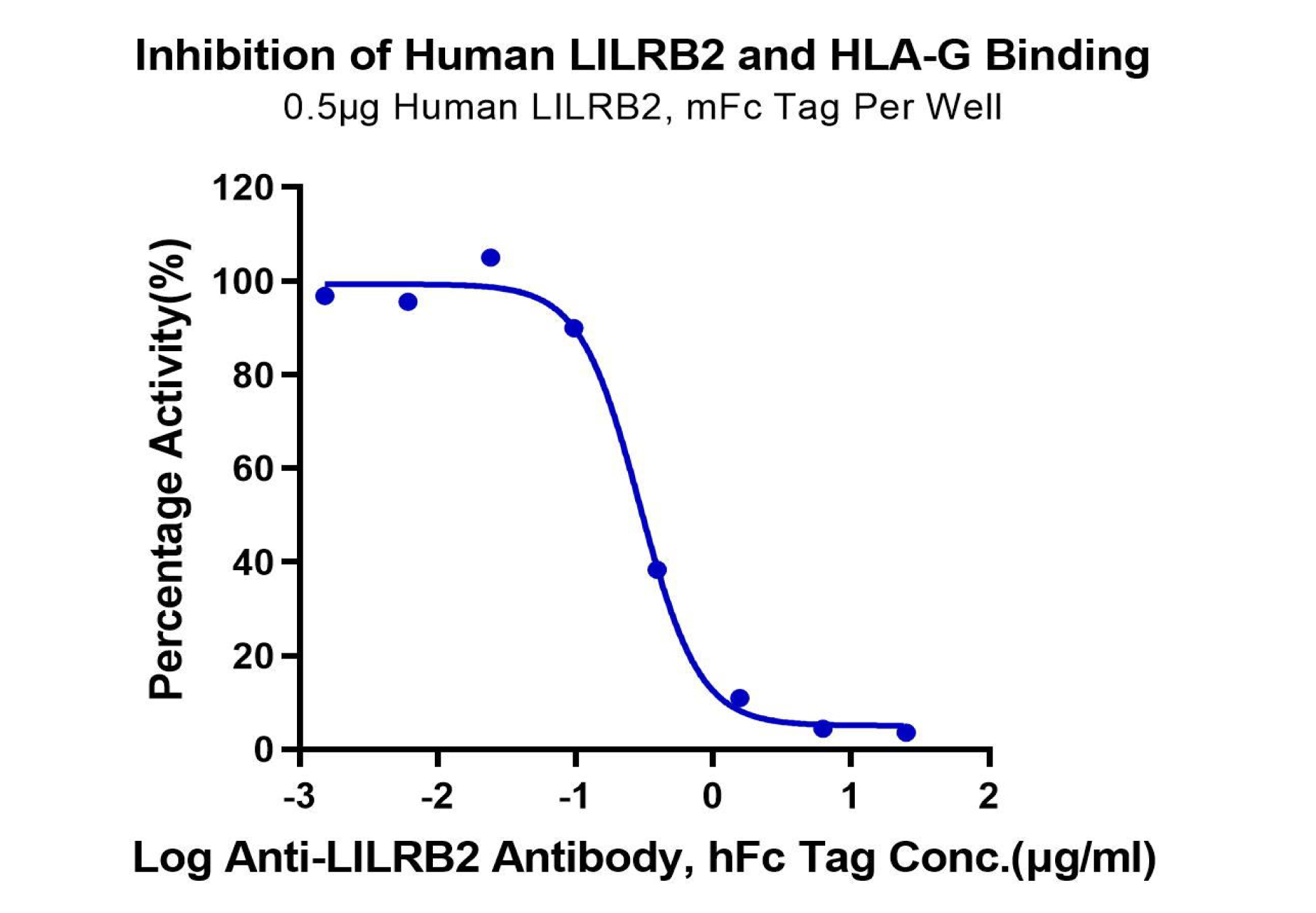


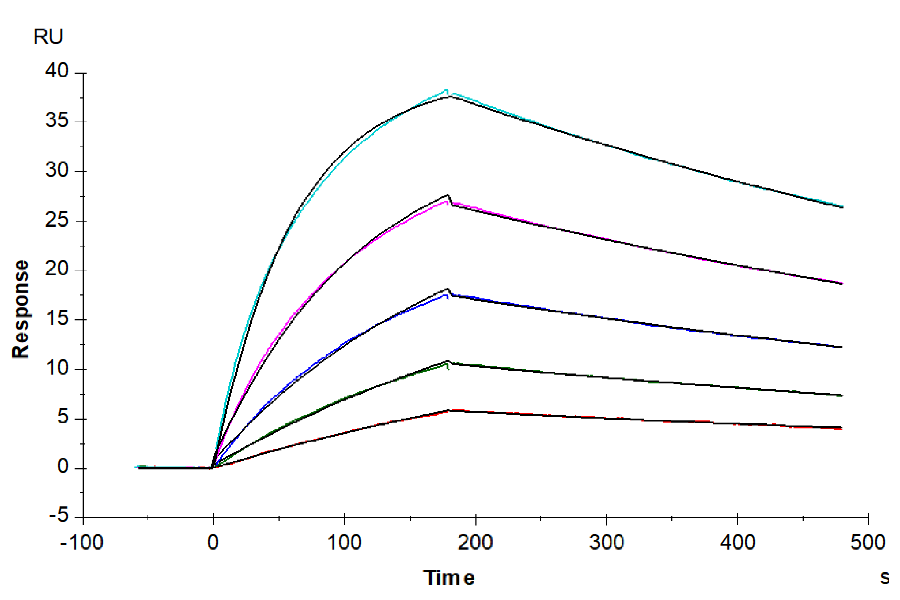
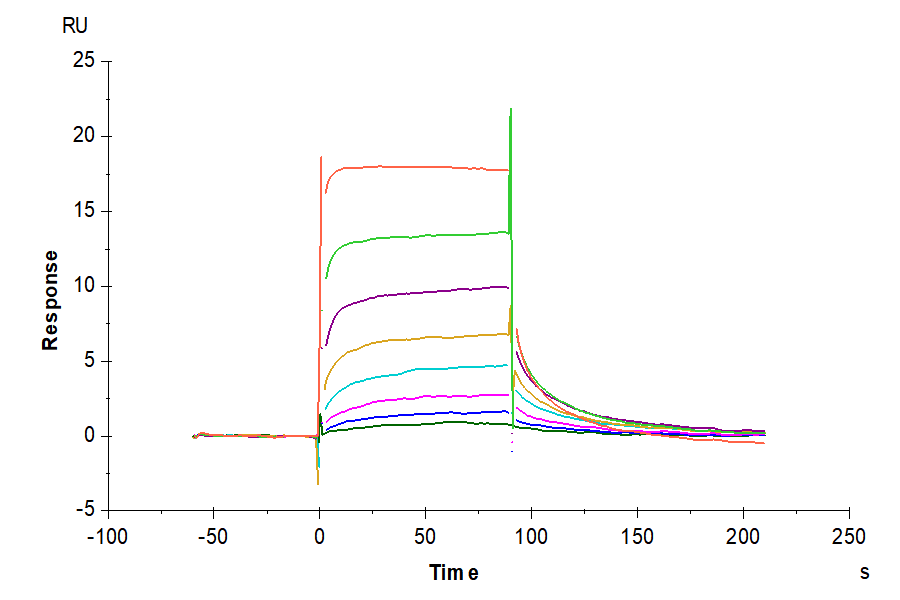

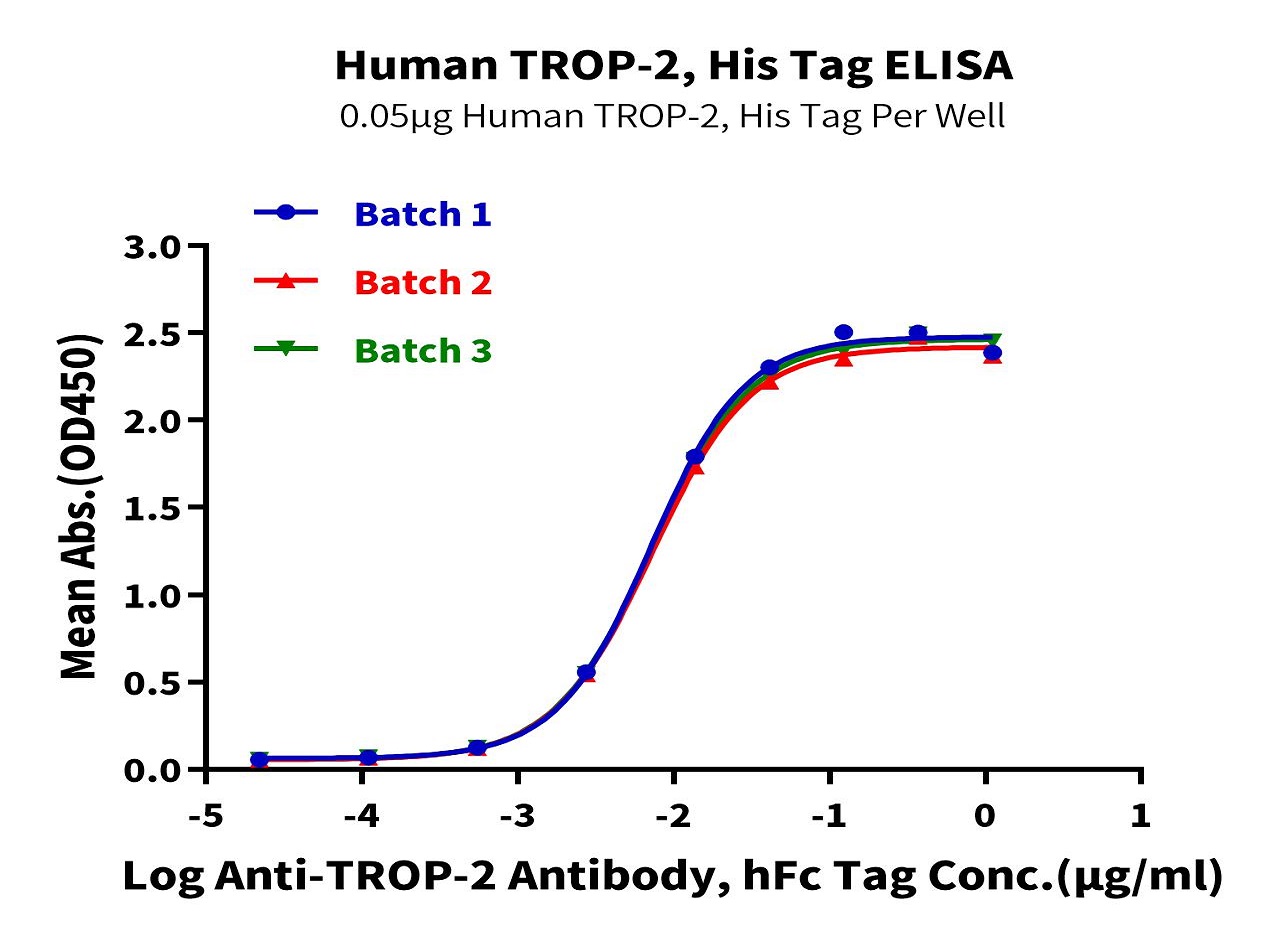
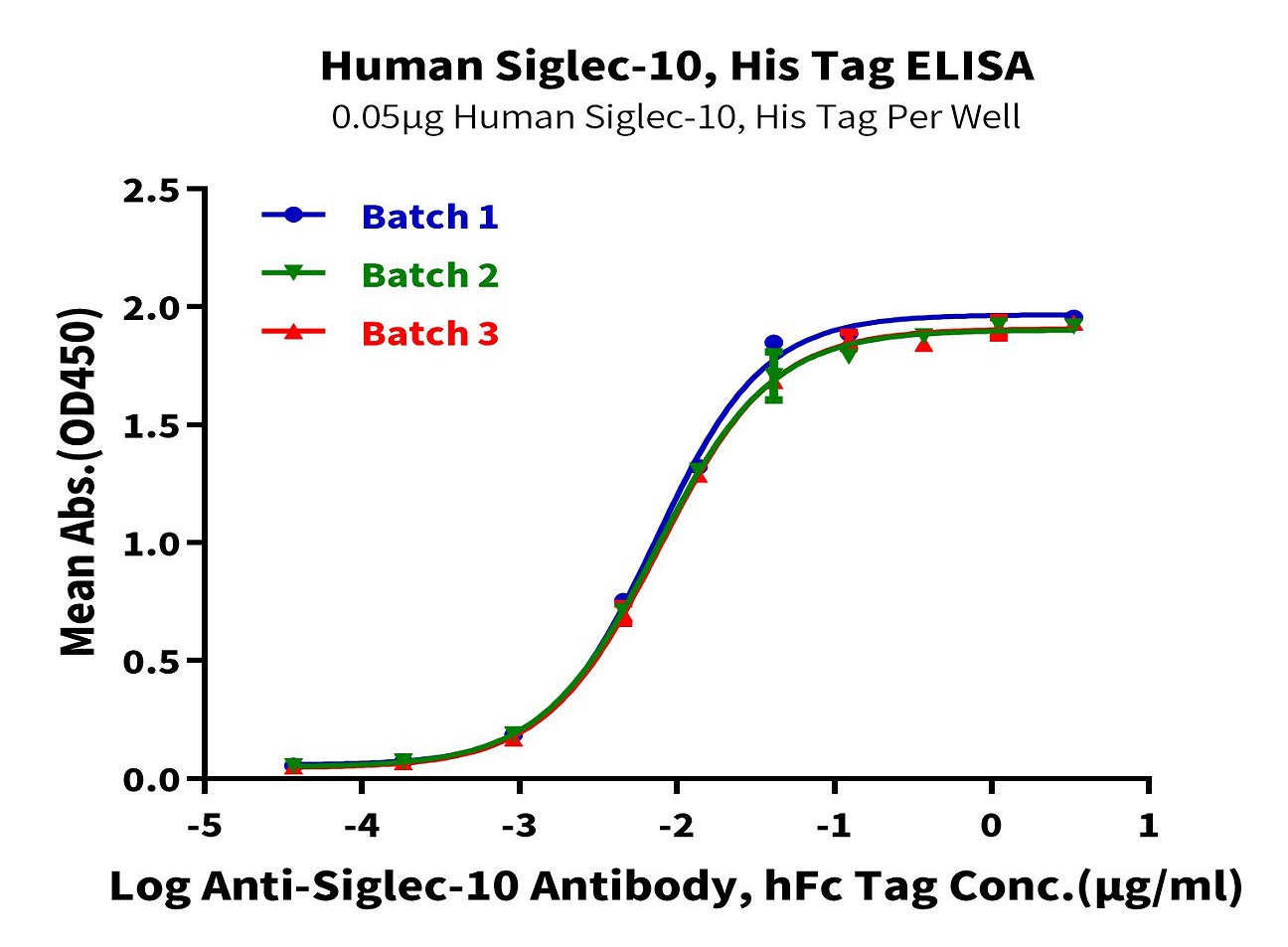
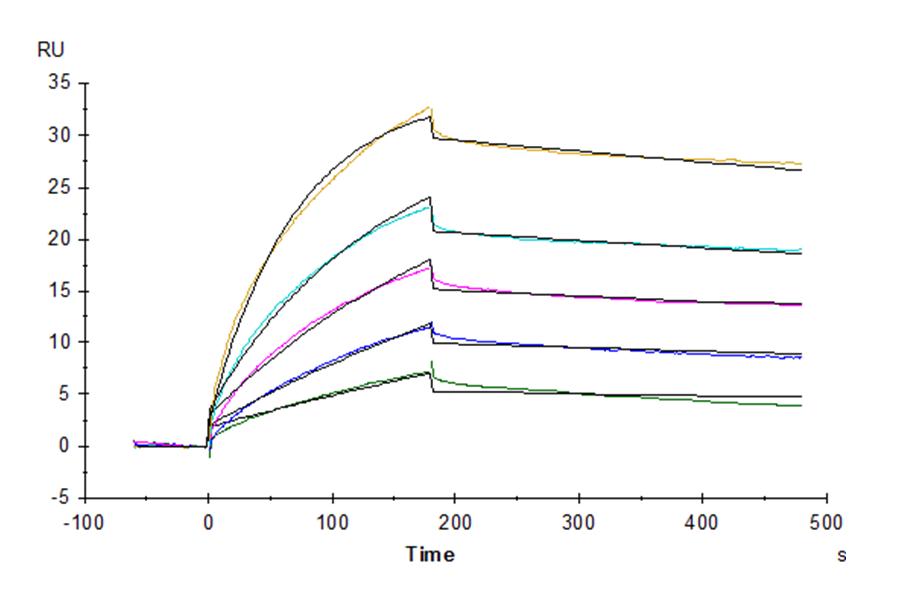
抗体药从研发到临床离不开严格的质量控制,需要高稳定性的优质蛋白确立生产控制参数,以确保方法的合理性及准确性,因而对所需蛋白的稳定性和活性提出了更高的要求。恺佧生物重组蛋白产品具备高度稳定性和优异的活性,可应用于抗体药的QC分析检测。数据示例:




针对不同的特殊需求,恺佧生物提供专业靶点蛋白定制服务,可为客户提供各种类型靶点蛋白及相关检测服务(如SPR分析),赋能客户的抗体药开发。以下是恺佧生物新型靶点蛋白定制一般流程:
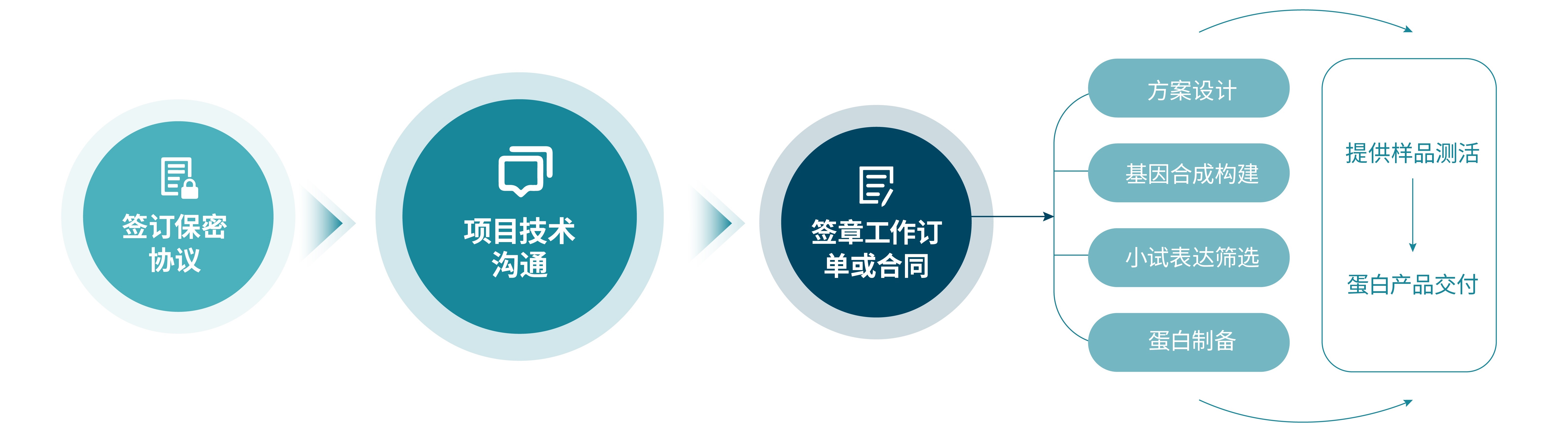
Fig. 11 恺佧生物靶点蛋白定制简要流程
抗体疗法已成为增长最快的治疗形式之一,各种新型抗体发现技术加速了抗体药进入临床的进程。随着越来越多的抗体药获批上市,癌症患者有望获得更长的生存期和更好的生活质量。恺佧生物将持续供应优质重组蛋白产品,为抗体药研究保驾护航,以使患者更快受益。

[1] Grewal Ys, Shiddiky MJ, Mahler SM,angelosi GA, Trau M. Nanoyeast and 0ther Cell Envelope Compositions for Protein Studies and Biosensor Applications ACS Appl Materlnterfaces. 2016 Nov 16:8(45):30649-30664.
[2] XueH,Bei Y, ZhanZ, ChenX XuX,Fu YV.Utilzing Biotinyated Proteins Expressed in Yeast to Visualize DNA-Protein lnteractions at the Single-Molecule level.Front Microbiol2017 0ct 24:8:2062.






