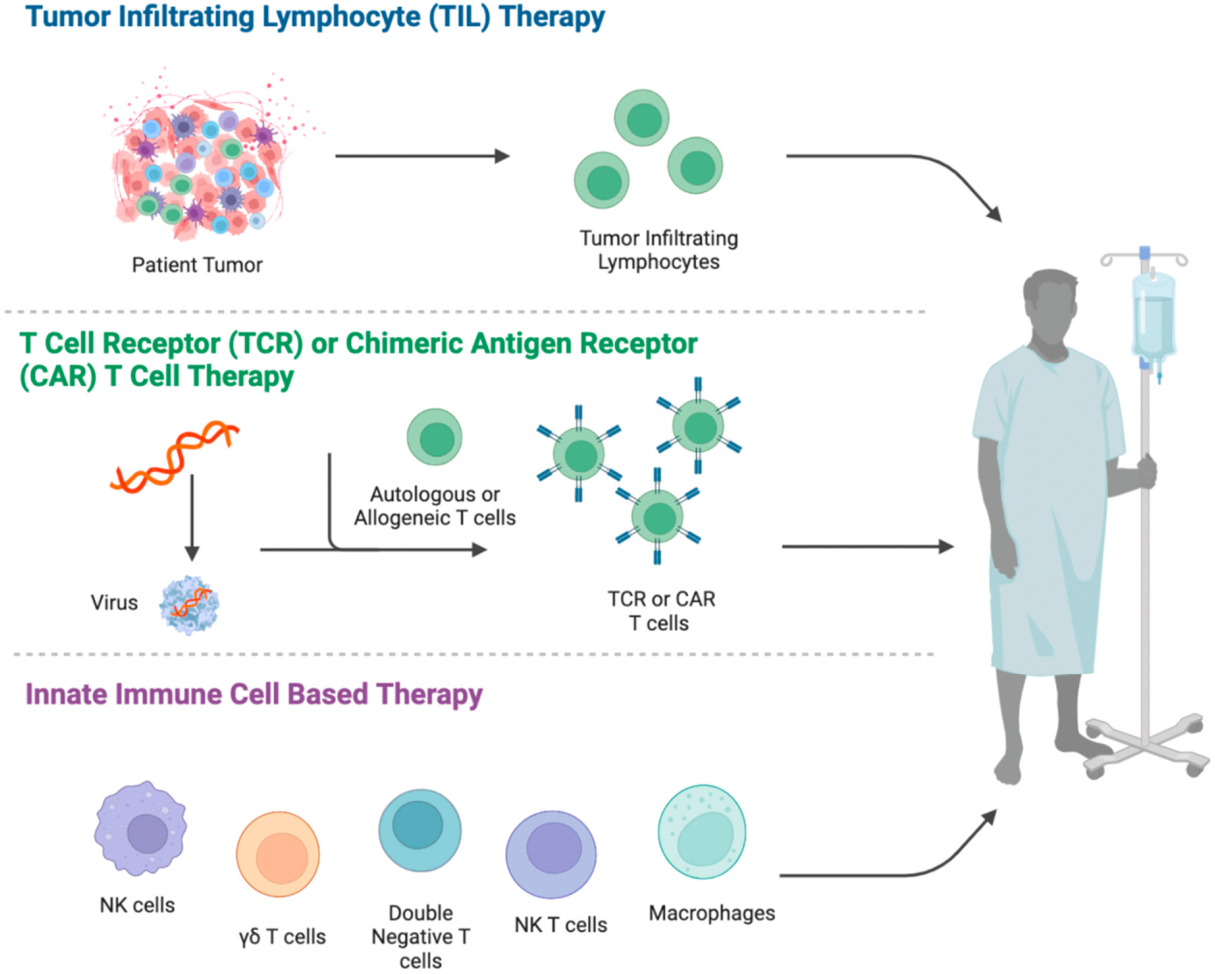
Fig. 1 免疫细胞治疗一般流程[1][2]



胞内抗原靶点是细胞治疗的一大方向。胞内抗原被降解后的肽段会与MHC形成复合物而被呈递在细胞表面以供TCR识别。通过靶向MHC多肽复合物,可实现肿瘤细胞的杀伤。
恺佧生物MHC多肽复合物涵盖诸多热门靶点,产品包括复合物单体、四聚体、荧光标记的四聚体等不同形式,可应用于T细胞治疗药物开发中的免疫或筛选等研究。同时提供TCR和TCR related drug等个性化定制表达服务,满足客户的多样需求。


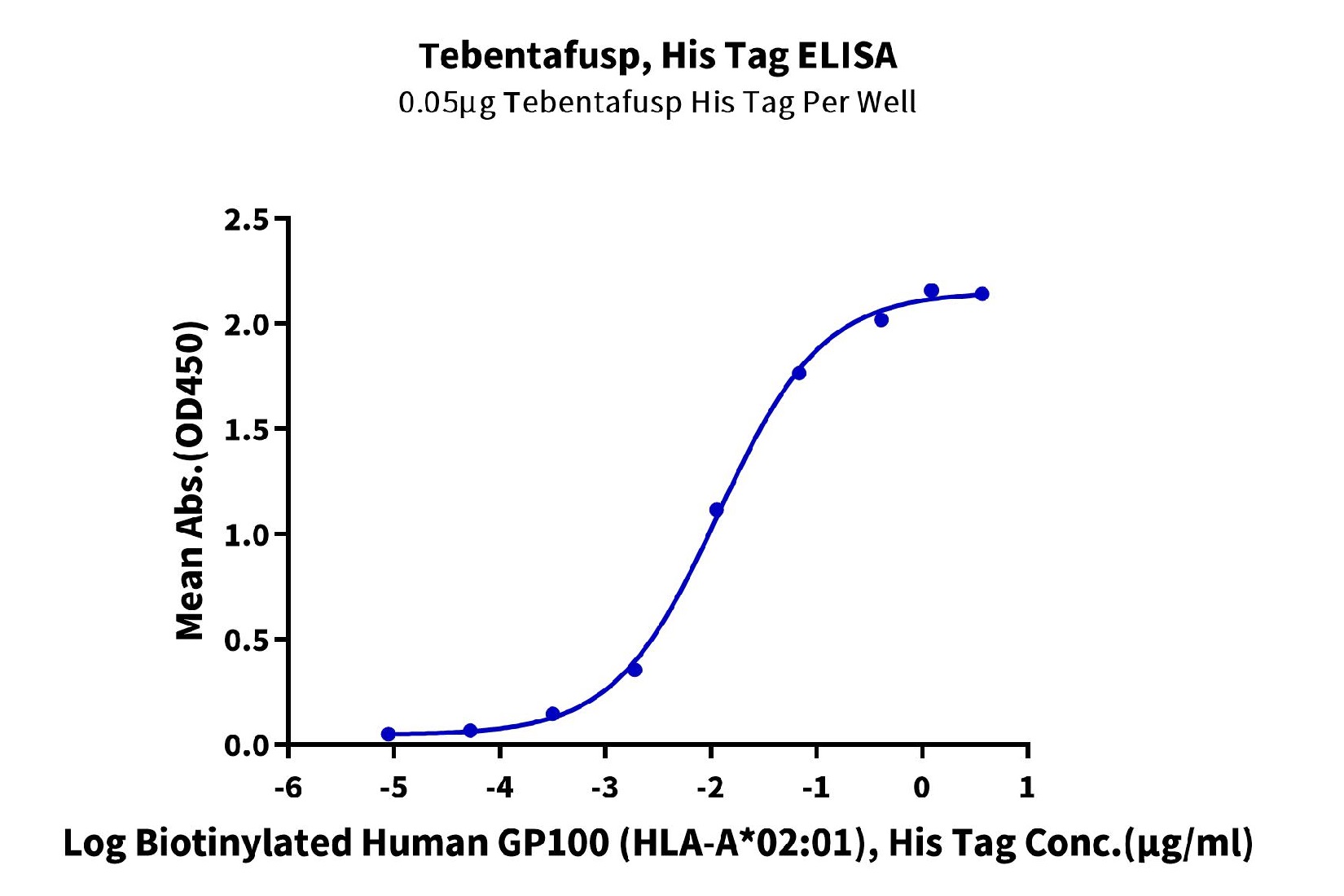
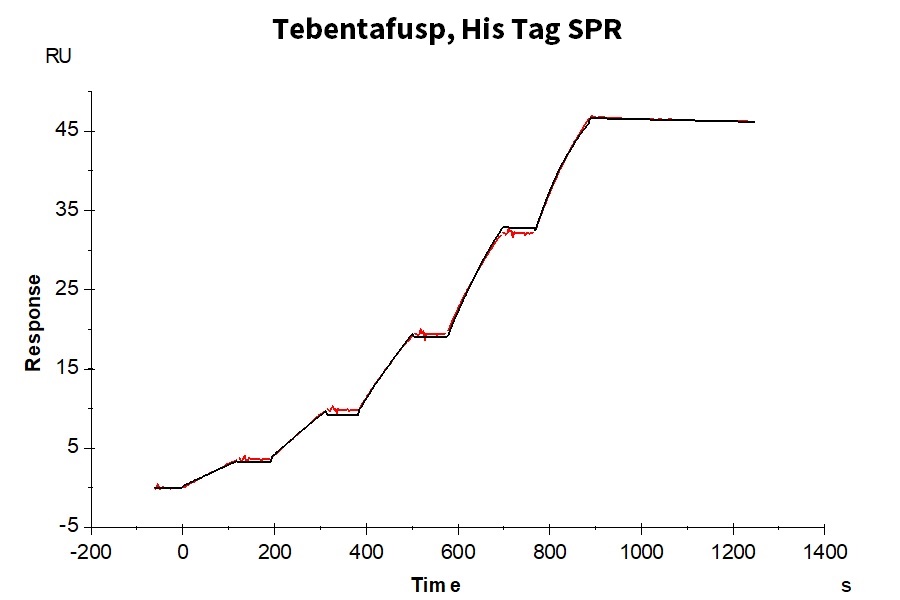

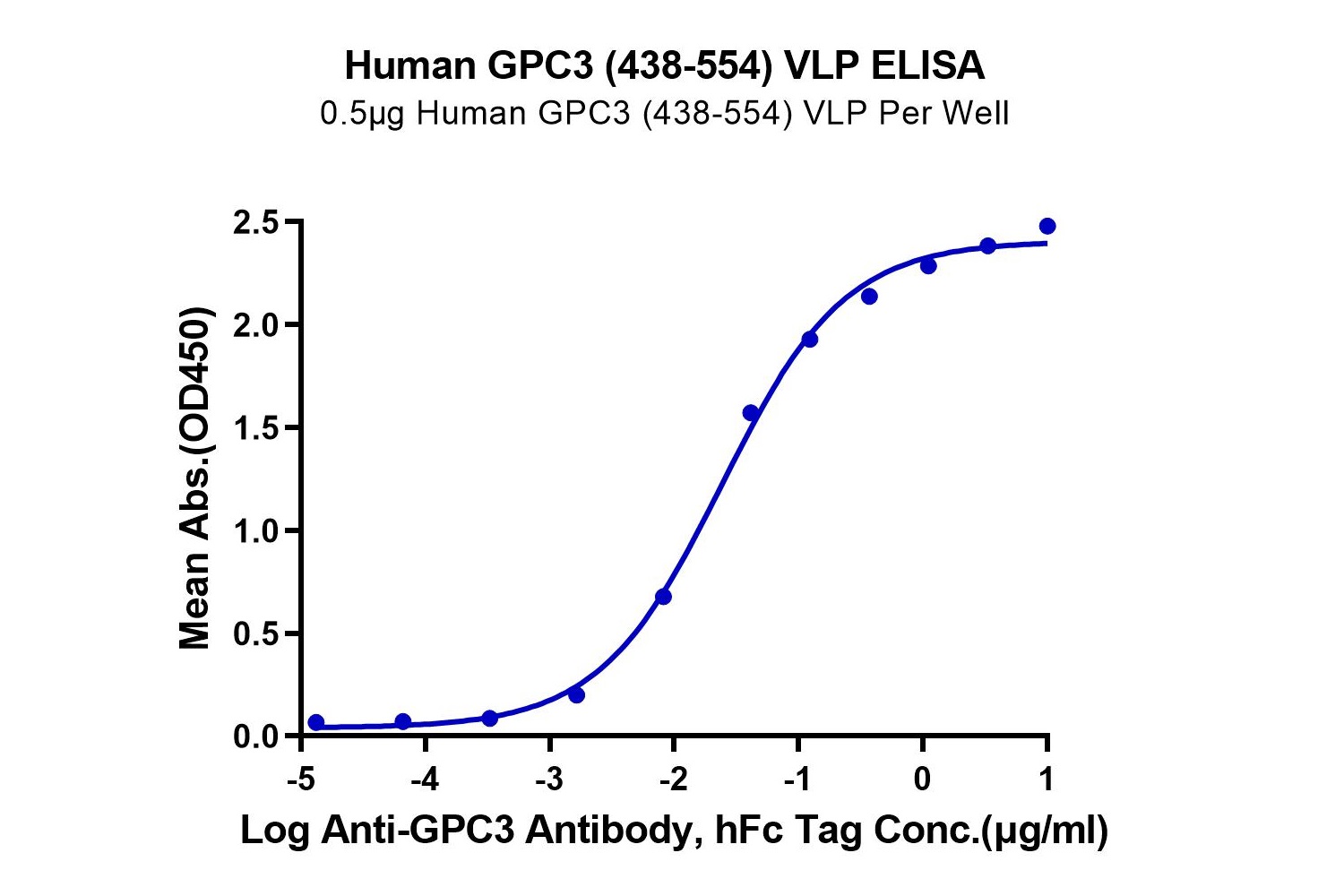
细胞疗法的靶点中包含了多次跨膜蛋白(如GPCR家族)以及一些通过直接免疫难以获得理想抗体序列的靶点。恺佧生物通过VLP展示技术,能更好地保持多次跨膜蛋白的正确构象,同时提高了蛋白的免疫原性。另外,针对不同的抗原可设计不同的VLP骨架,并可提供个性化定制服务。



细胞培养是细胞药物顺利进行生产制备的保证,如免疫细胞治疗过程中T细胞、NK细胞和干细胞源性免疫细胞治疗中所需的干细胞的培养,以及干细胞治疗中ESC、MSC、iPSC的培养等。

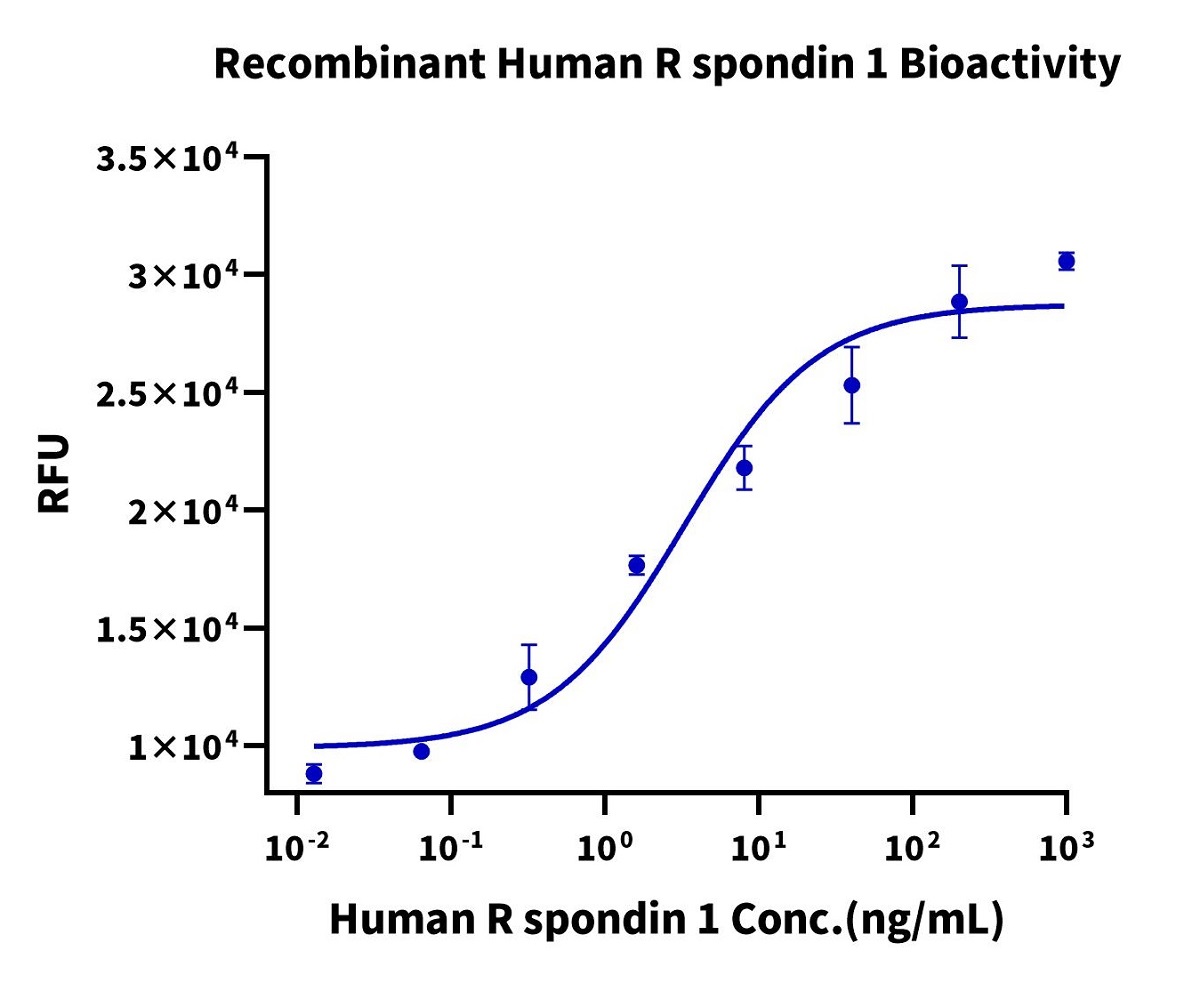
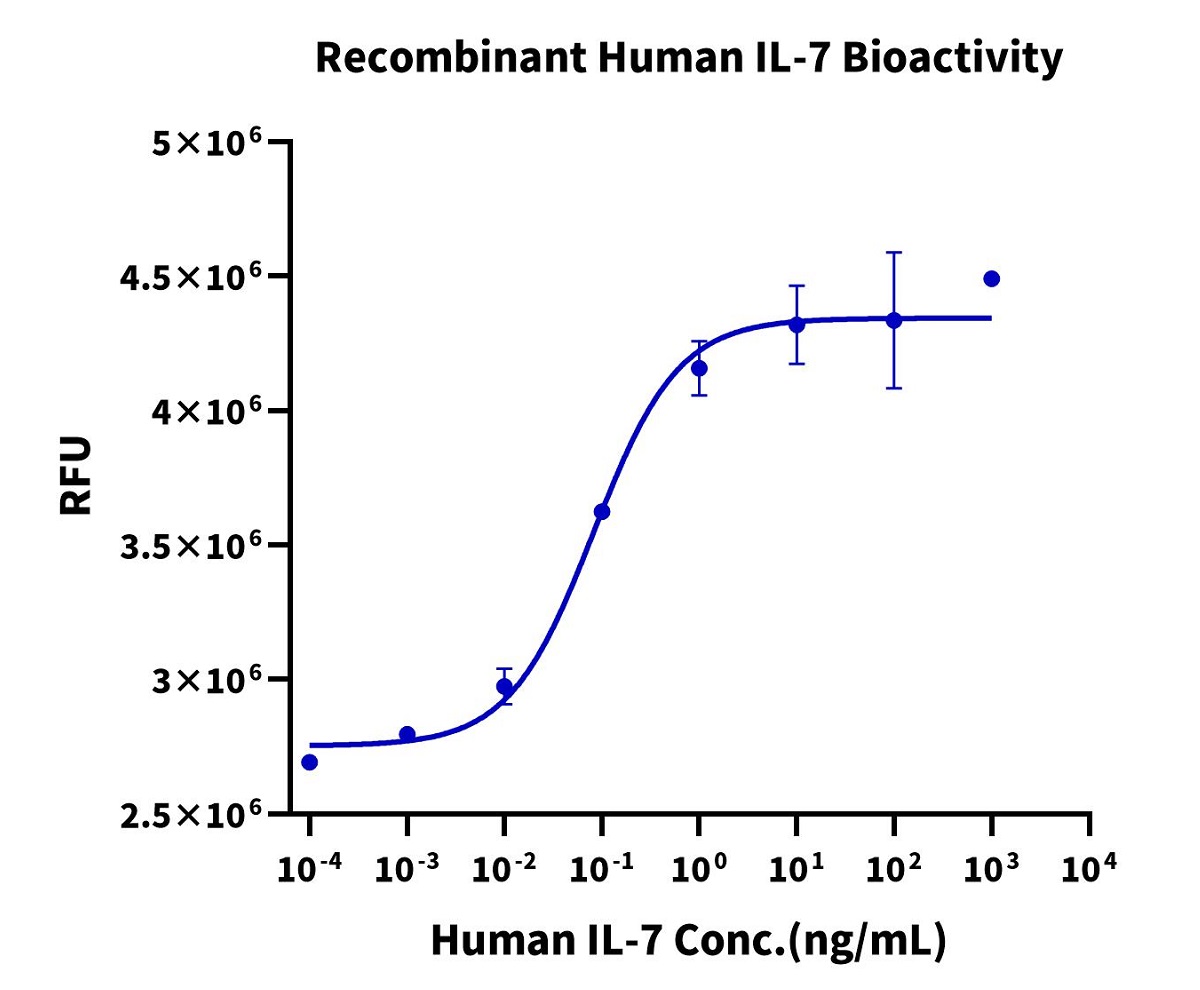
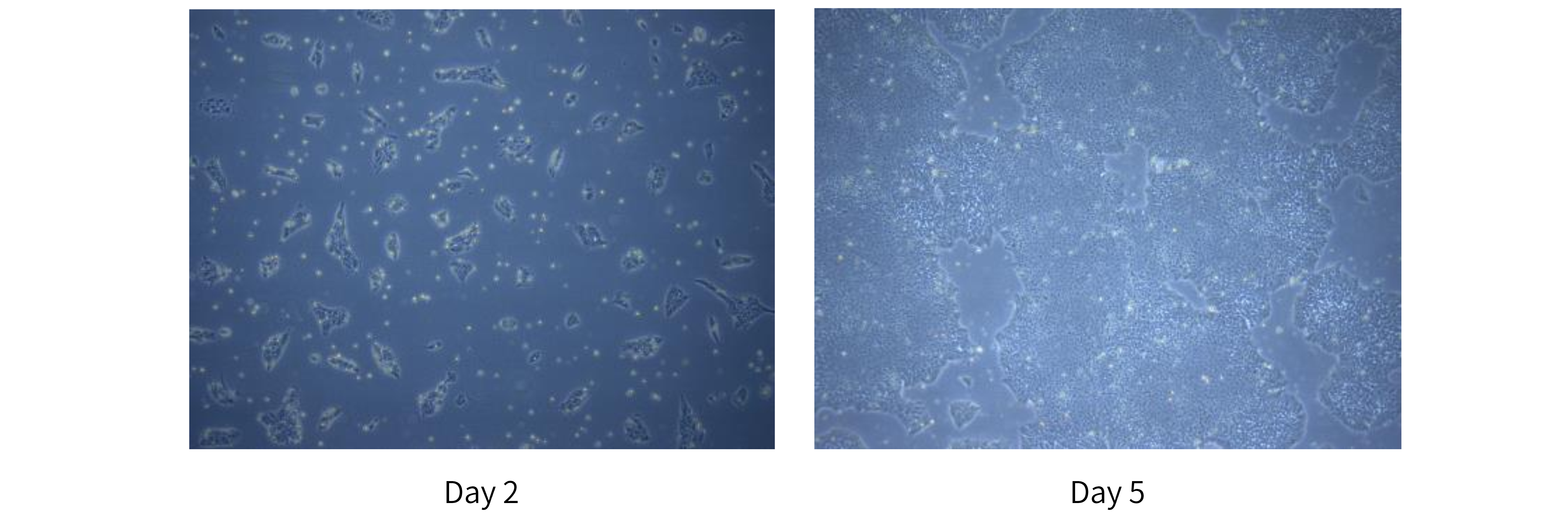
Fig. 12 细胞培养基质蛋白Laminin 521能有效促进人iPSC的生长
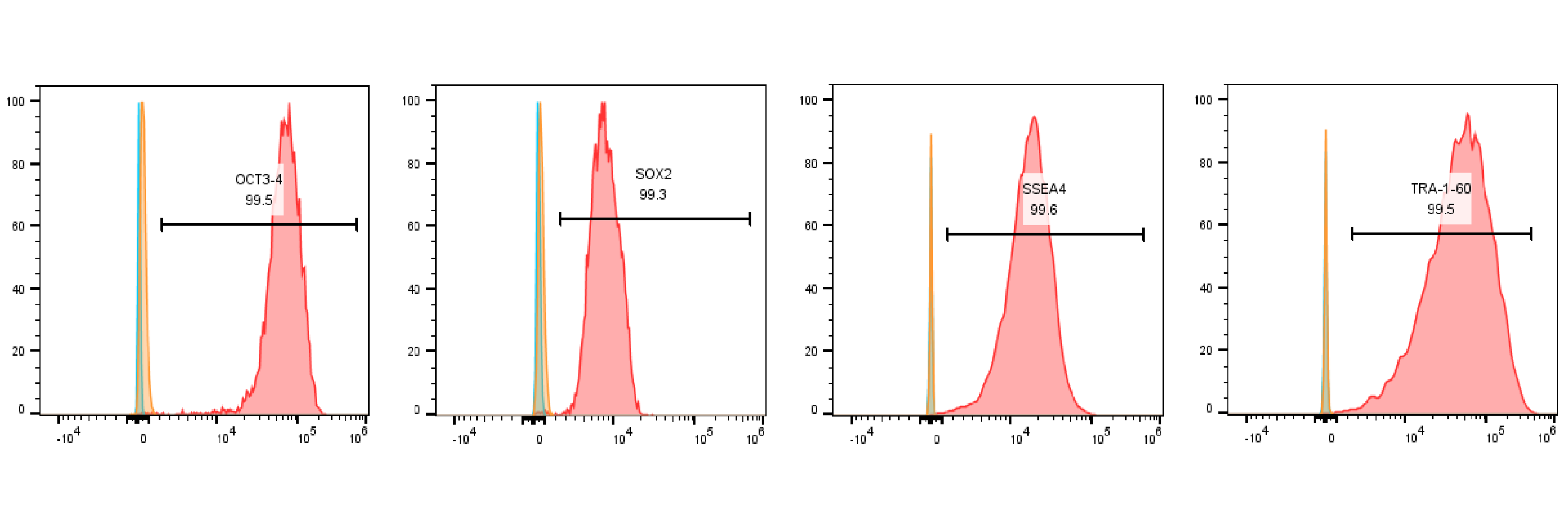
Fig. 13 细胞培养基质蛋白Laminin 521可维持干细胞分化潜能

荧光或生物素标记的蛋白可用于治疗性细胞生产制备和质检中的多种检测过程,如抗体筛选(如scFv等)、CAR亲和力研究、CAR-T阳性率检测、TCR筛选或检测,以及Blocking Assay等,恺佧生物提供高质量FITC、PE等不同荧光标记以及生物素标记的蛋白等,满足细胞水平在内的不同分析场景。
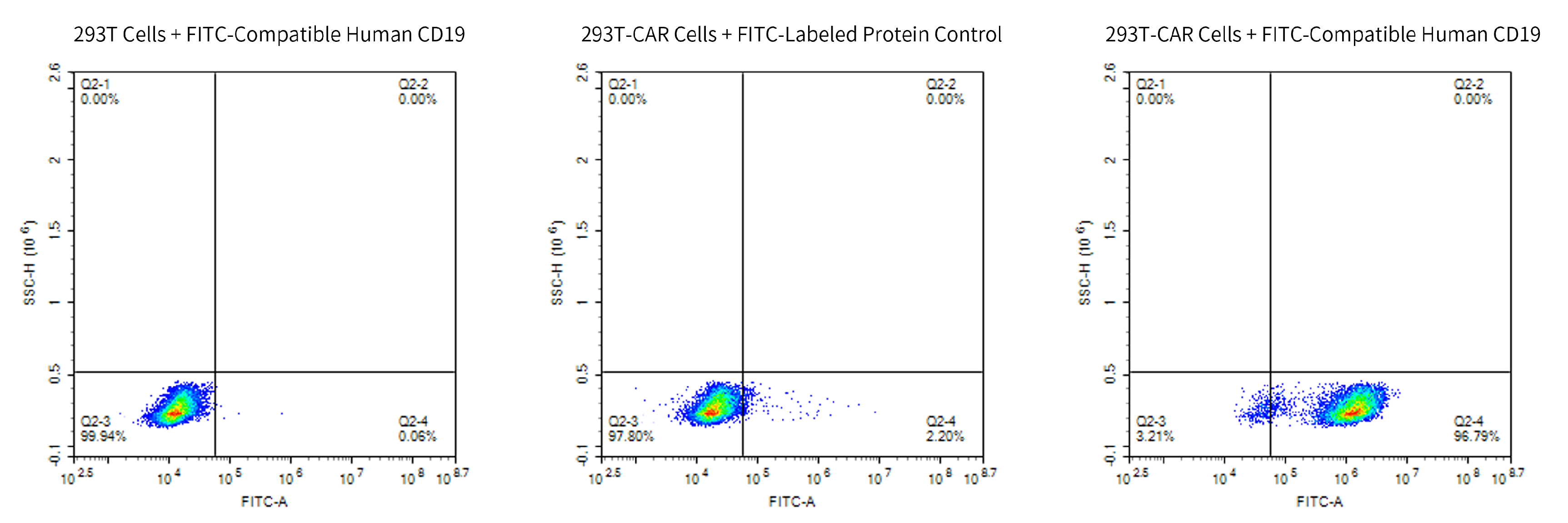
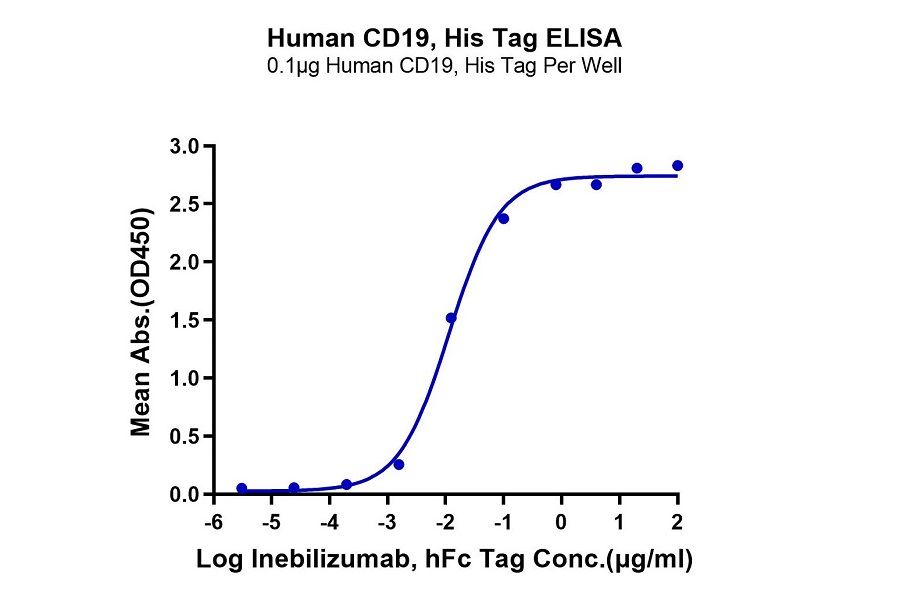
Fig. 14 经细胞水平流式检测,FITC-Compatible Human CD19 protein可和Anti-CD19-CAR T细胞特异性结合。

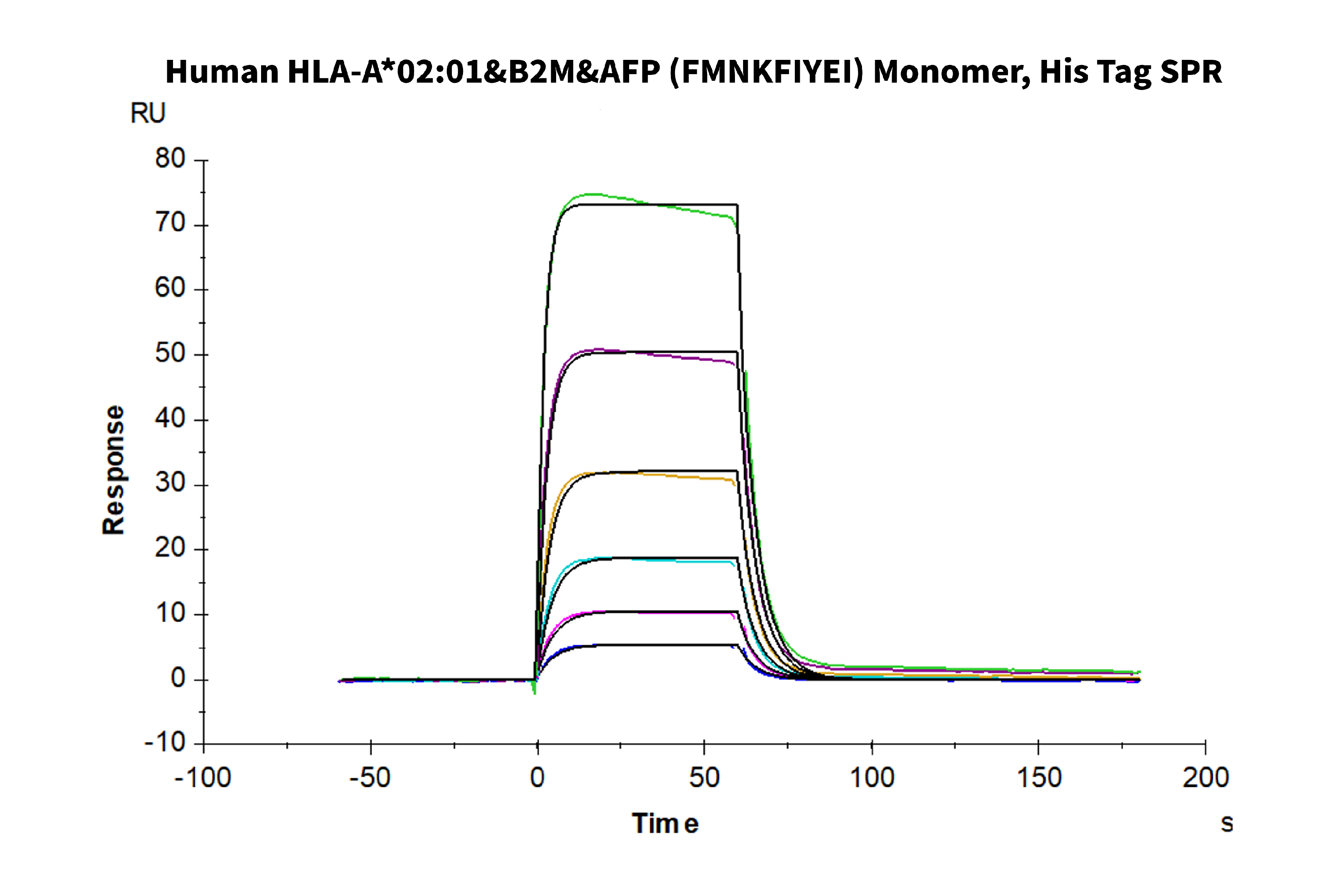
Fig. 15 经细胞水平流式检测,荧光标记的HLA-A*02:01&B2M&NY-ESO-1 (SLLMWITQC)复合物四聚体可很好地与HLA-A*02:01&B2M&NY-ESO-1 TCR细胞结合。

同种异体通用型细胞治疗产品,如UCAR-T,需通过基因编辑技术,敲除供体T细胞上与免疫排斥反应相关的基因,避免引起GvHD和HvGR等免疫排斥反应。恺佧生物提供Cas9、Cas12a、hfCas12Max®等基因编辑核酸酶,可用于UCAR-T细胞治疗药物的基因修饰。其中,GMP级别的Cas9核酸酶已完成DMF备案(编号:036578),可协助客户完成IND申报。

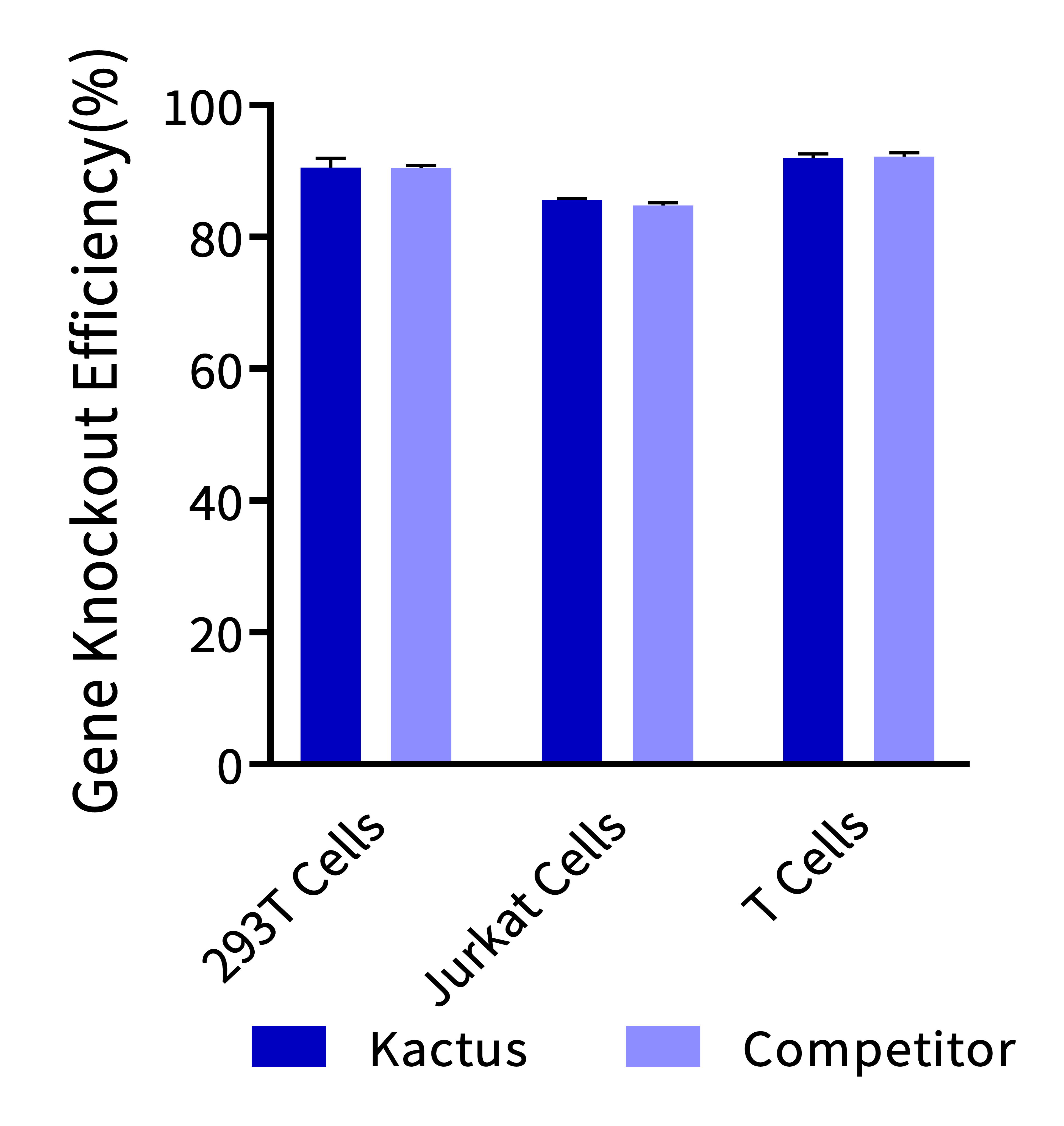
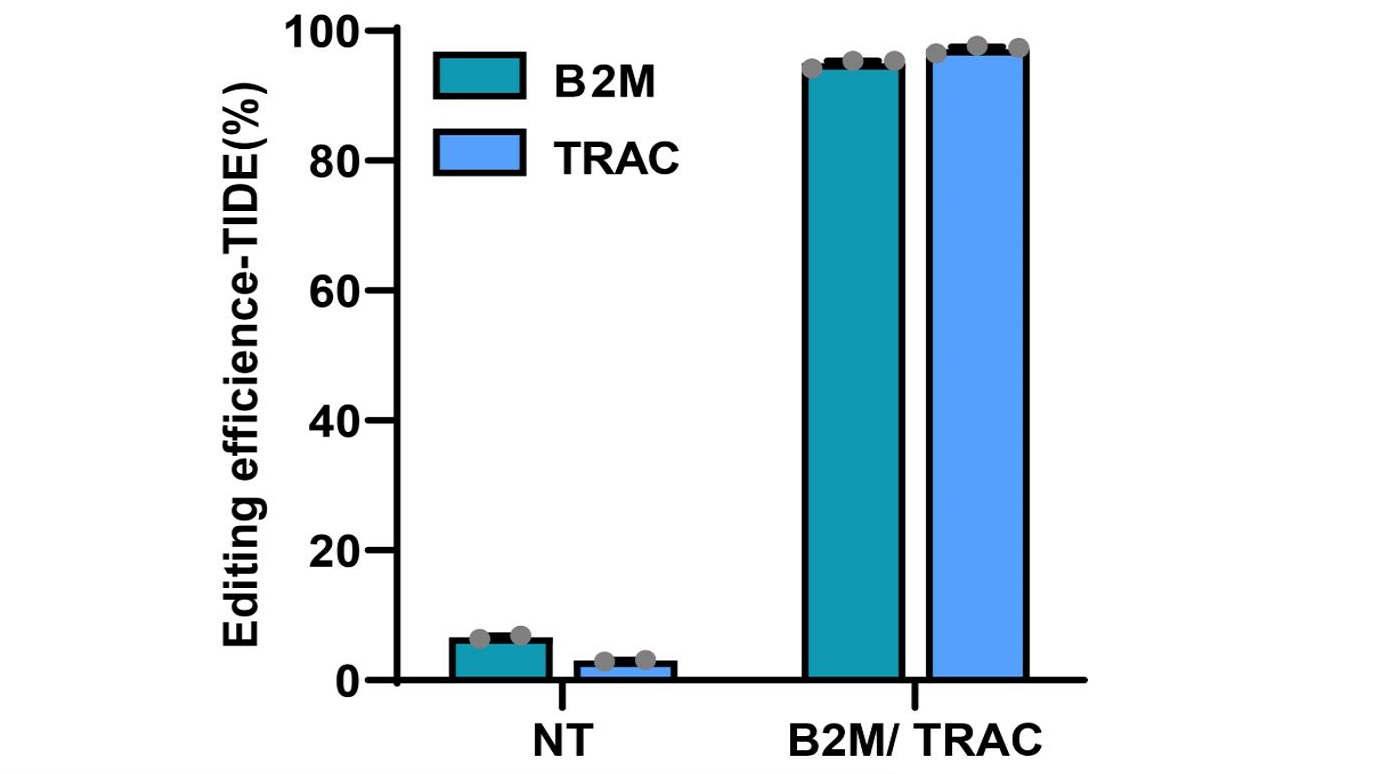


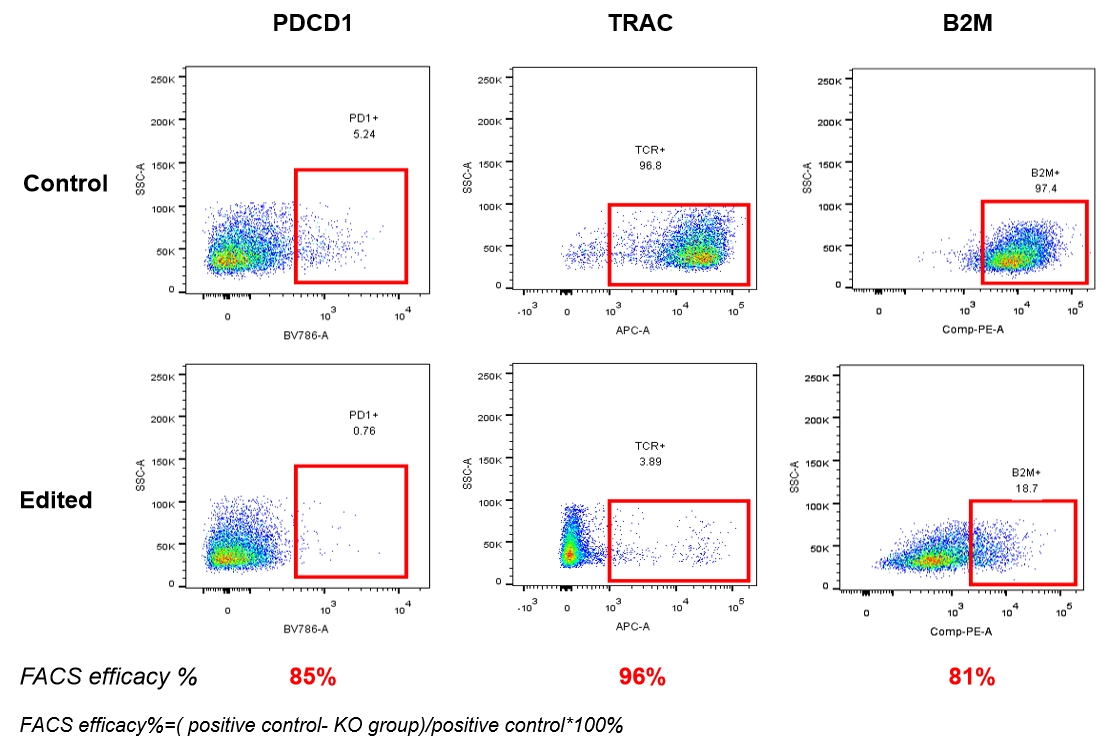
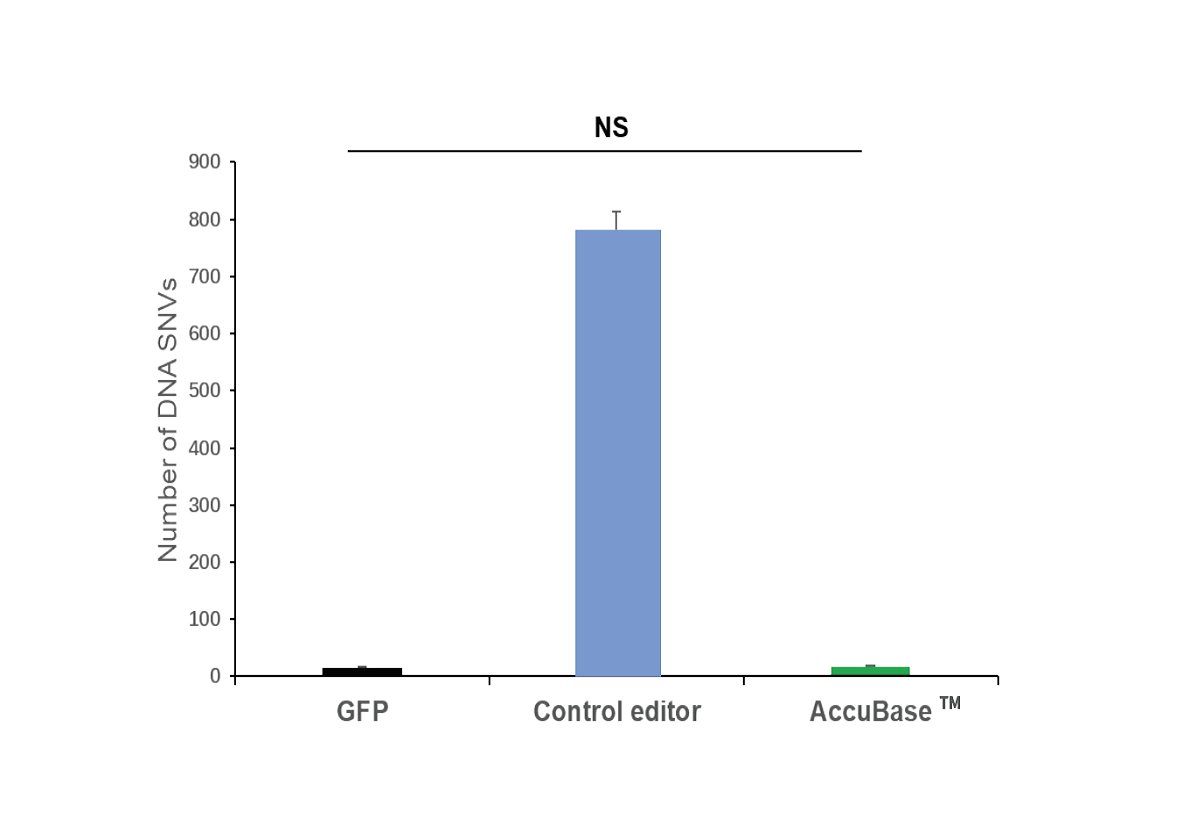
碱基编辑蛋白相较于基因编辑酶,在编辑的过程中不会引入DSB,确保了编辑的安全性。AccuBase®是通过基因工程手段设计的CBE,将窗口范围内的 C 脱氨形成 U,U利用细胞内修复机制转变为 T,从而实现C→T的转变。此外,创造性地将脱氨酶可逆的包裹起来,只有当 sgRNA 与靶位点结合时才能发挥脱氨作用,大幅度降低了与非靶 DNA 的随机结合,可以实现接近零脱靶的效果,同时维持高效的编辑活性。

定量检测基因编辑细胞药物在回输人体之前胞外或胞内中Cas9核酸酶的残留。试剂盒检测范围为0.25 ng/ml-16 ng/ml,灵敏度可达0.125 ng/ml。


Fig. 22 多项式拟合标准曲线,R2达到0.9997。

在细胞治疗领域,主要用于药物生产过程中去除宿主DNA和质粒DNA等杂质,MaxNuclease全能核酸酶于高标准的CGT蛋白酶GMP生产车间生产,不使用含动物源原材料,分析方法经系统验证,并经过全方位的QC放行检测,满足从研发到商业大规模生产的使用需求,已完成DMF备案(编号:036799)。
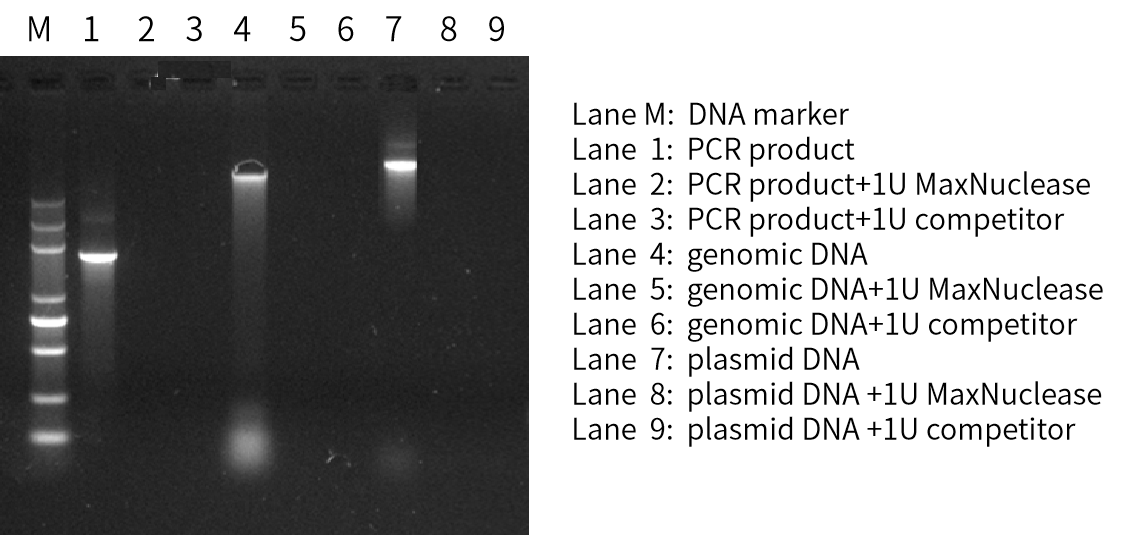
Fig. 23 MaxNuclease降解核酸效果

定量检测细胞治疗药物中全能核酸酶的残留,试剂盒检测范围为46.88 pg/ml-3000 pg/ml,灵敏度可达23.44 pg/ml。


Fig. 24 线性拟合标准曲线,R2达到0.9995。
| 货号 | 产品名称 | 规格 | |
| KACTUS-CAS9 | Cas9 Nuclease | 1 mg/3 mg | 立即询价 |
| KACTUS-CAS9-GMP | Cas9 Nuclease(GMP grade) | 3 mg | 立即询价 |
| CAS-MM00B | Cas9 (CRISPR Associated Protein 9) ELISA Kit | 96 T | 立即询价 |
| CAS-EE111 | SpCas9 D10A Nickase | 1 mg | 立即询价 |
| CAS-EE121 | AsCas12a Nuclease | 1 mg | 立即询价 |
| CAS-EE128 | hfCas12Max® | 500 μg/1 mg | 立即询价 |
| KD-0001 | BS-EP1(Trade name: AccuBase®) | 200 μg/500 μg/1 mg | 立即询价 |
| GMP-KD-0001 | BS-EP1(Trade name: AccuBase®), GMP grade | 1 mg | 立即询价 |
| NUC-SE101 | MaxNuclease全能核酸酶 | 50 kU/250 kU/5 MU | 立即询价 |
| GMP-NUC-SE101 | MaxNuclease全能核酸酶(GMP grade) | 250 kU/5 MU | 立即询价 |
| NUC-SE00B | MaxNuclease ELISA Kit | 96 T | 立即询价 |

[1] Fang KK, Lee JB, Zhang L. Adoptive Cell Therapy for T-Cell Malignancies. Cancers (Basel). 2022 Dec 23;15(1):94.
[2] Mangal JL, Handlos JL, Esrafili A, Inamdar S, Mcmillian S, Wankhede M, Gottardi R, Acharya AP. Engineering Metabolism of Chimeric Antigen Receptor (CAR) Cells for Developing Efficient Immunotherapies. Cancers (Basel). 2021 Mar 5;13(5):1123.
[3] Maalej KM, Merhi M, Inchakalody VP, Mestiri S, Alam M, Maccalli C, Cherif H, Uddin S, Steinhoff M, Marincola FM, Dermime S. CAR-cell therapy in the era of solid tumor treatment: current challenges and emerging therapeutic advances. Mol Cancer. 2023 Jan 30;22(1):20.